《医疗器械经营许可证》提交材料目录.doc
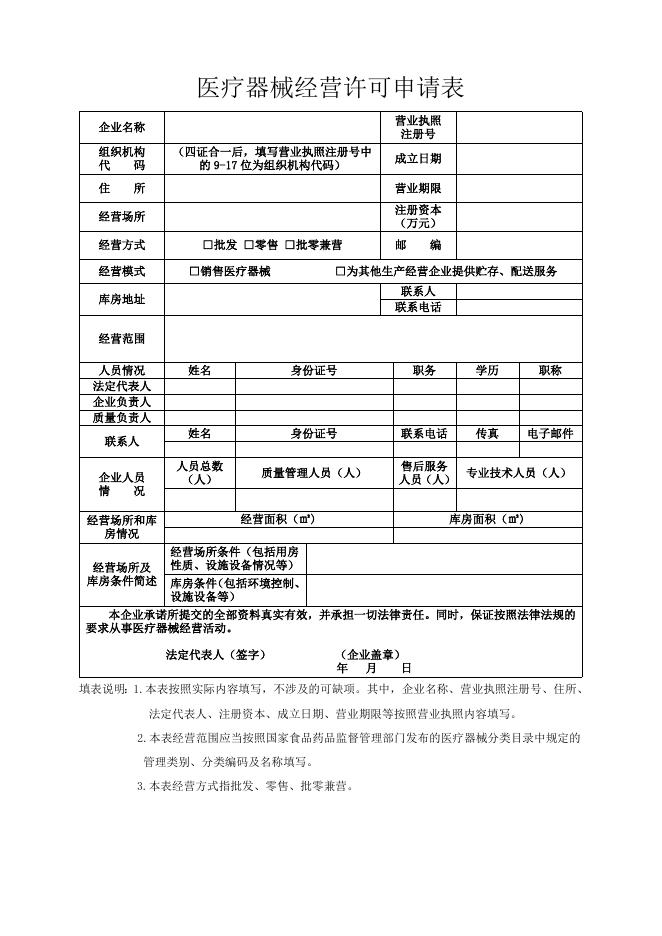
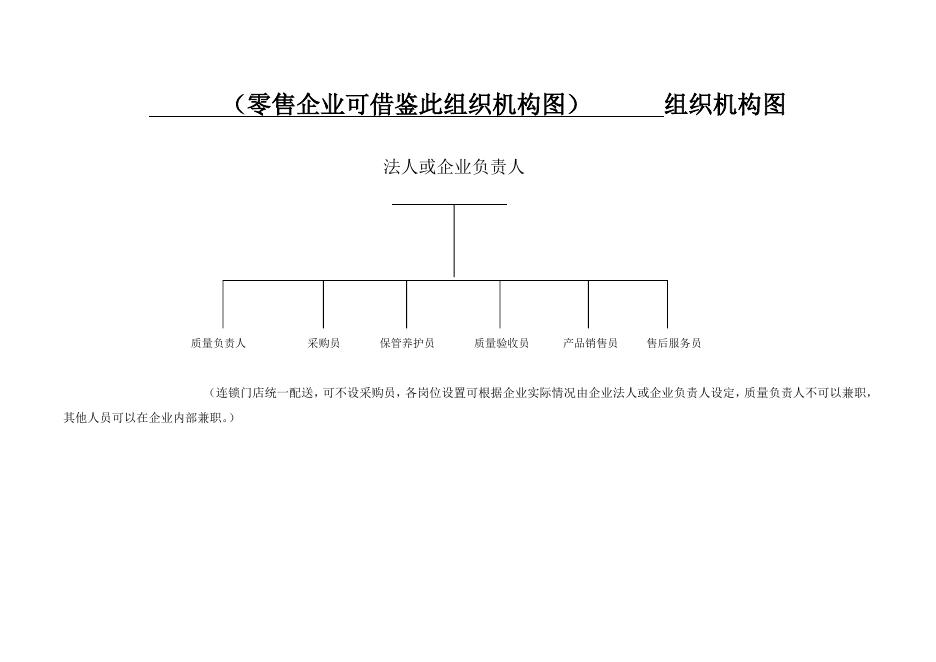
申请《医疗器械经营许可证》提交材料目录 1、申报材料目录及页码; 2、医疗器械经营许可申请表; 3、营业执照正、副本复印件; 4、法定代表人、企业负责人、质量负责人身份证明、学历或 者职称证明复印件; 5、组织机构与部门设置说明; 6、经营范围、经营方式说明; 7、经营场所、库房地址的地理位置图(标清街道和门牌号 等)、平面图(注明面积和区域划分)、房屋产权证明文件或者租 赁协议(附房屋产权证明文件)复印件(如经营场所和库房地址 与住所为同一地址,可仅提供位置图与平面图,不需提供产权证 明及租赁协议。) ; 8、经营设施、设备目录; 9、经营质量管理制度、工作程序等文件目录; 10、计算机信息管理系统基本情况介绍和功能说明; 11、经办人授权证明。 卷 内 目 录 企业名称: 联系电话: 编号 注:所有材料必须加盖公章。 联系人: 内 容 页 码 医疗器械经营许可申请表 营业执照 注册号 企业名称 组织机构 代 码 住 (四证合一后,填写营业执照注册号中 的 9-17 位为组织机构代码) 成立日期 所 营业期限 经营场所 注册资本 (万元) 经营方式 □批发 □零售 □批零兼营 经营模式 □销售医疗器械 邮 编 □为其他生产经营企业提供贮存、配送服务 联系人 联系电话 库房地址 经营范围 人员情况 法定代表人 企业负责人 质量负责人 联系人 企业人员 情 况 经营场所和库 房情况 经营场所及 库房条件简述 姓名 身份证号 职务 学历 职称 姓名 身份证号 联系电话 传真 电子邮件 人员总数 (人) 质量管理人员(人) 售后服务 专业技术人员(人) 人员(人) 经营面积(㎡) 库房面积(㎡) 经营场所条件(包括用房 性质、设施设备情况等) 库房条件(包括环境控制、 设施设备等) 本企业承诺所提交的全部资料真实有效,并承担一切法律责任。同时,保证按照法律法规的 要求从事医疗器械经营活动。 法定代表人(签字) (企业盖章) 年 月 日 填表说明:1.本表按照实际内容填写,不涉及的可缺项。其中,企业名称、营业执照注册号、住所、 法定代表人、注册资本、成立日期、营业期限等按照营业执照内容填写。 2.本表经营范围应当按照国家食品药品监督管理部门发布的医疗器械分类目录中规定的 管理类别、分类编码及名称填写。 3.本表经营方式指批发、零售、批零兼营。 营业执照正、副本复印件(略) (营业执照的经营范围中应包含医疗器械销售) (如未办理四证合一,需同时提供组织机构代码证正、副本复印 件) 法定代表人、企业负责人、质量负责人身份证、毕业证或 者职称证复印件(略) (零售企业可借鉴此组织机构图) 组织机构图 法人或企业负责人 质量负责人 采购员 保管养护员 质量验收员 产品销售员 售后服务员 (连锁门店统一配送,可不设采购员,各岗位设置可根据企业实际情况由企业法人或企业负责人设定,质量负责人不可以兼职, 其他人员可以在企业内部兼职。 ) (批发企业可借鉴此组织机构图) 组织机构图 法人或企业负责人 质量负责人(或质管部长): 经理(或销售部长):XXX 办公室主任:XXX XXX 质量管理员 质量验收员 保管养护员 采购员 产品销售员 售后服务员 运输员 财务 (各部门和岗位设置可根据企业实际情况由企业法人或企业负责人设定;企业质量管理人数是指质量负责人和质量管理员的和,企业质量管理人员不可 以兼职,企业质量管理人数应与其经营规模和经营范围相适应;企业其他人员可以在企业内部兼职。) (零售企业) 部门名称 部门设置说明(表一) 岗位职责说明 法人或企业负责 内容结合企业制定的质量管理制度和《医疗器械经营质量管理 规范》来填写。 人 质量负责人 采购员 质量验收员 保管养护员 产品销售员 售后服务员 备 注 (批发企业) 部门设置说明(表一) 部门名称 部门职能说明 法人或企业负责 内容结合企业制定的质量管理制度和《医疗器械经营质量管理 规范》来填写。 人 根据企业组织机 构实际设置填写 备 注 部门设置说明(表二) 医疗器械经营企业从业人员基本情况表 填报单位(盖章) 序 号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 姓名 职务 学历 专业 职称 身份证号 XXX 公司经营范围、经营方式说明 我公司拟经营的产品名称为 XXX、XXX,注册证为:XXX、XXX, 按照国家食品药品监督管理总局颁布的医疗器械分类目录,以上 产品的管理类别为三类。因此,我公司的经营范围确定为:Ⅲ类 医疗器械:XXX:XXX(类代号及名称) 、XXX:XXX。 我公司拟将以上产品销售给(任选其一:具有资质的经营企 业或医疗机构、或是直接销售给消费者、或是既销售给具有资质 的经营企业和医疗机构又销售给消费者) ,因此,我公司的经营方 式为(与上面对应选择其一:批发、零售、或批零兼营) 。 (现场检查时,按照《医疗器械经营质量管理规范》要求, 核实相关产品资质、供方资质及授权) 经营场所、库房地址的地理位置图(标清街道和门牌号等) 、 室内平面图(注明面积和区域划分,库房需标明各分区设置情 况)、房屋产权证明文件或者租赁协议(附房屋产权证明文件)复 印件。 (略) 如企业经营场所和库房地址与住所地址一致,可不提供产权 证明文件或租赁协议(附房屋产权证明文件)复印件,仅提供位 置图和平面图。 现场库房设置:待验区为黄色、合格品区为绿色、发货区为 绿色、不合格品区为红色、退货产品单独存放。 零售企业可不设库房。 经营设施、设备目录 序号 名 称 型 号 精 度 数 量 用 途 经营质量管理制度目录 (三类批发企业) (一)质量管理机构或者质量管理人员的职责; (二)质量管理的规定; (三)采购、收货、验收的规定(包括采购记录、验收记录、随货同行单等); (四)供货者资格审核的规定(包括供货者及产品合法性审核的相关证明文件 等); (五)库房贮存、出入库管理的规定(包括温度记录、入库记录、定期检查记录、 出库记录等); (六)销售和售后服务的规定(包括销售人员授权书、购货者档案、销售记录 等); (七)不合格医疗器械管理的规定(包括销毁记录等); (八)医疗器械退、换货的规定; (九)医疗器械不良事件监测和报告规定(包括停止经营和通知记录等); (十)医疗器械召回规定(包括医疗器械召回记录等); (十一)设施设备维护及验证和校准的规定(包括设施设备相关记录和档案等); (十二)卫生和人员健康状况的规定(包括员工健康档案等); (十三)质量管理培训及考核的规定(包括培训记录等); (十四)医疗器械质量投诉、事故调查和处理报告的规定(包括质量投诉、事故 调查和处理报告相应的记录及档案等)。 (十五)购货者资格审核、医疗器械追踪溯源、质量管理制度执行情况考核的规 定; (十六)质量管理自查制度的规定; (十七)质量管理记录制度的规定。 工作程序目录 (三类批发企业) 1、质量管理文件管理程序 2、医疗器械采购工作程序 3、医疗器械验收工作程序 4、医疗器械贮存及养护工作程序 5、医疗器械出库管理及复核工作程序 6、医疗器械运输工作程序 7、医疗器械销售工作程序 8、医疗器械售后服务工作程序 9、不合格品处置工作程序 10、购进退出及销后退回管理工作程序 11、不良事件报告工作程序 12、医疗器械召回工作程序 经营质量管理制度目录 (三类零售企业) (一)质量管理机构或者质量管理人员的职责; (二)质量管理的规定; (三)采购、收货、验收的规定(包括采购记录、验收记录、随货同行单等); (四)供货者资格审核的规定(包括供货者及产品合法性审核的相关证明文件 等); (五)专柜贮存、定期检查的规定(包括温度记录、定期检查记录等); (六)销售和售后服务的规定(包括销售记录等); (七)不合格医疗器械管理的规定(包括销毁记录等); (八)医疗器械退、换货的规定; (九)医疗器械不良事件监测和报告规定(包括停止经营和通知记录等); (十)医疗器械召回规定(包括医疗器械召回记录等); (十一)设施设备维护及验证和校准的规定(包括设施设备相关记录和档案等); (十二)卫生和人员健康状况的规定(包括员工健康档案等); (十三)质量管理培训及考核的规定(包括培训记录等); (十四)医疗器械质量投诉、事故调查和处理报告的规定(包括质量投诉、事故 调查和处理报告相应的记录及档案等)。 (十五)购货者资格审核、医疗器械追踪溯源、质量管理制度执行情况考核的规 定; (十六)质量管理自查制度的规定; (十七)质量管理记录制度的规定。 工作程序目录 (三类零售企业) 1、质量管理文件管理程序 2、医疗器械采购工作程序 3、医疗器械验收工作程序 4、医疗器械贮存及定期检查工作程序 5、医疗器械销售工作程序 6、医疗器械售后服务工作程序 7、不合格品处置工作程序 8、购进退出及销后退回管理工作程序 9、不良事件报告工作程序 10、医疗器械召回工作程序 质量管理制度目录 (验配类角膜接触镜及其护理液经营企业) (一)质量管理机构或者质量管理人员的职责; (二)质量管理的规定; (三)采购、收货、验收的规定(包括采购记录、验收记录、随货同行单等); (四)供货者资格审核的规定(包括供货者及产品合法性审核的相关证明文件 等); (五)专柜贮存、管理的规定(包括定期检查记录等); (六)销售和售后服务的规定(包括验配操作程序、验配服务管理、购货者档案、 销售记录等); (七)不合格医疗器械管理的规定(包括销毁记录等); (八)医疗器械退、换货的规定; (九)医疗器械不良事件监测和报告规定(包括停止经营和通知记录等); (十)医疗器械召回规定(包括医疗器械召回记录等); (十一)设施设备维护及验证和校准的规定(包括设施设备相关记录和档案等); (十二)卫生和人员健康状况的规定(包括员工健康档案等); (十三)质量管理培训及考核的规定(包括培训记录等); (十四)医疗器械质量投诉、事故调查和处理报告的规定(包括质量投诉、事故 调查和处理报告相应的记录及档案等)。 (十五)医疗器械追踪溯源、质量管理制度执行情况考核的规定; (十六)质量管理自查制度的规定; (十七)质量管理记录制度的规定。 工作程序目录 (验配类角膜接触镜及其护理液经营企业) 1、质量管理文件管理程序 2、医疗器械采购工作程序 3、医疗器械验收工作程序 4、医疗器械专柜贮存及定期检查工作程序 5、医疗器械验配及销售工作程序 6、医疗器械售后服务工作程序 7、不合格品处置工作程序 8、购进退出及销后退回管理工作程序 9、不良事件报告工作程序 10、医疗器械召回工作程序 计算机信息管理系统基本情况介绍和功能说明 我公司使用的计算机信息管理系统名称为:XXX,其具有以下 功能: (一)具有实现部门之间、岗位之间信息传输和数据共享的 功能; (二)具有医疗器械经营业务票据生成、打印和管理功能; (三)具有记录医疗器械产品信息(名称、注册证号或者备 案凭证编号、规格型号、生产批号或者序列号、生产日期或者失 效日期)和生产企业信息以及实现质量追溯跟踪的功能; (四)具有包括采购、收货、验收、贮存、检查、销售、出 库、复核等各经营环节的质量控制功能,能对各经营环节进行判 断、控制,确保各项质量控制功能的实时和有效; (五)具有供货者、购货者以及购销医疗器械的合法性、有 效性审核控制功能; (六)具有对库存医疗器械的有效期进行自动跟踪和控制功 能,有近效期预警及超过有效期自动锁定等功能,防止过期医疗 器械销售。 经办人授权证明 大庆市食品药品监督管理局: 是我公司 人员,现委托其在大 庆市食品药品监督管理局办理医疗器械相关证件事宜,其间出现 任何问题,由我公司承担一切法律责任。 授权范围: □1、接受行政机关依法告知的权利。 □2、代为提交申请材料、更正、补正、补充材料的权利。 □3、代理申请人行政许可审查中的陈述和申辩的权利。 □4、签收相关文书和证件的权利。 □5、其他权利 。 注:已授权的请在□中打“√”,未授权的请在□中打“×” 。 委托期限自 年 月 被委托人身份证正面 复印件粘贴处 日至 年 月 被委托人身份证背面 复印件粘贴处 企业名称(公章):XXXXXXX 公司 法人签字: 日。 年 月 日

 《医疗器械经营许可证》提交材料目录.doc
《医疗器械经营许可证》提交材料目录.doc